Physique des membranes biologiques
Membres
- Miglena Anguelova, enseignante-chercheuse
- Jean-Baptiste Manneville, chercheur
- Nicolas Puff, enseignant-chercheur
- Chandini Bhaskar-Naidu, doctorante
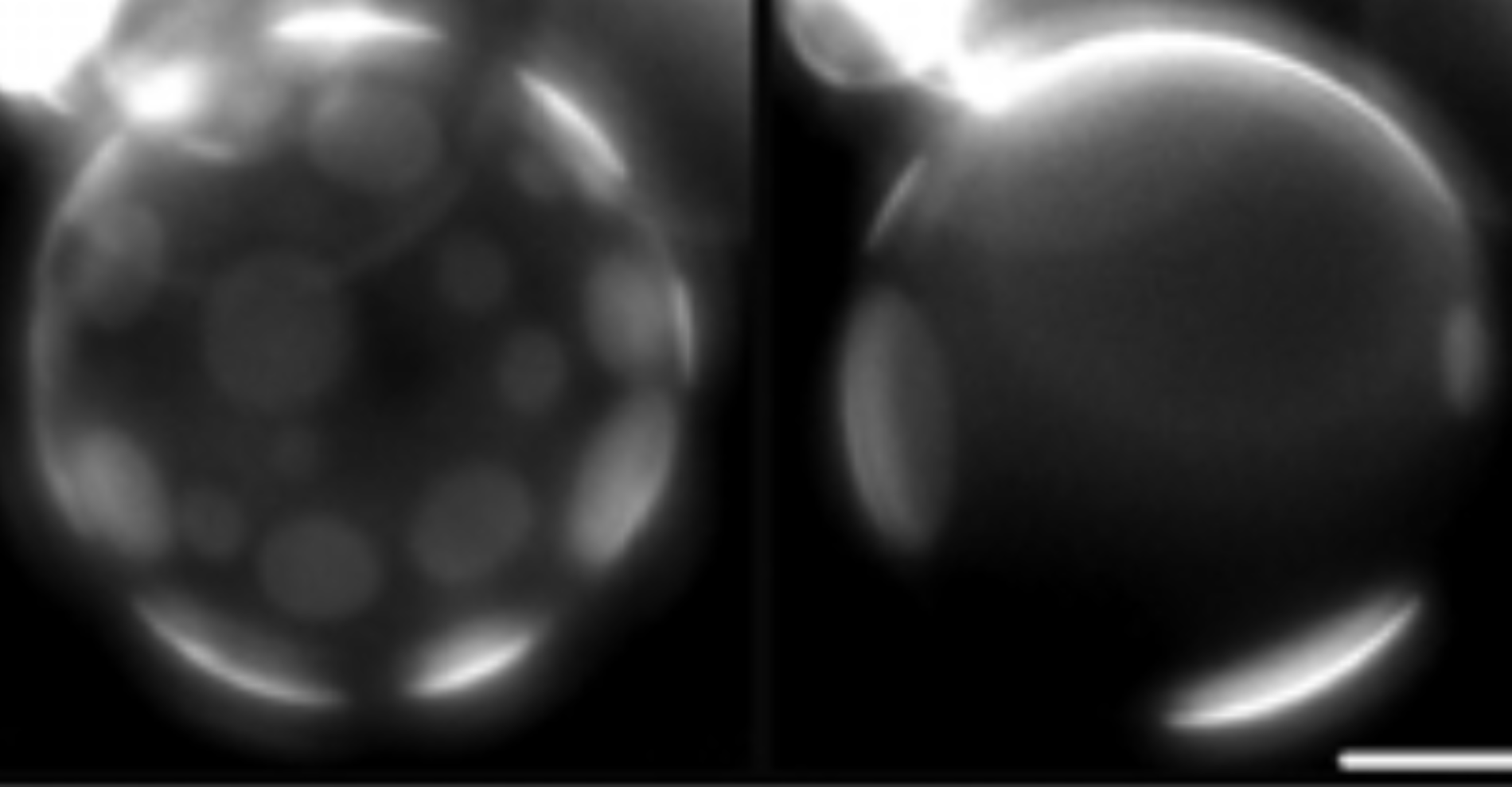
Membranes modèles
Nous développons des systèmes modèles expérimentaux de la cellule vivante, reproduisant la structure hétérogène de la membrane lipidique et sa dynamique induite par la création, dans son proche environnement, de gradients de composition chimique, ainsi que la déformation directionnelle d’une bicouche lipidique guidée par un gradient chimique localisé. Actuellement nous sommes très intéressés par certains aspects physicochimiques et membranaires dans la maladie d’Alzheimer, ainsi que par la mécano toxicité de l’Amyloid beta et les effets croisés de la maladie d’Alzheimer et des cancers.
Pour en savoir plus
Quelques articles
Dynamique des membranes biologiques
Mitochondrial Cristae Architecture and Functions: Lessons from Minimal Model Systems. Joubert, F., Puff, N., 2021. Membranes 11, 465.
Improved Characterization of Raft-Mimicking Phase-Separation Phenomena in Lipid Bilayers Using Laurdan Fluorescence with Log-Normal Multipeak Analysis. Puff, N., Staneva, G., Angelova, M.I., Seigneuret, M., 2020. Langmuir 36, 4347–4356.
pH Sensing by Lipids in Membranes: The Fundamentals of pH-driven Migration, Polarization and Deformations of Lipid Bilayer Assemblies. Angelova MI, Bitbol A-F, Seigneuret M, Staneva G, Kodama A, Sakuma Y, Kawakatsu T, Imai M, Puff N, 2018, Review article in Special Issue “Emergence of Complex Behavior in Biomembranes”, Ed. Longo M. BBA-Biomembranes 1860 , 2042–2063
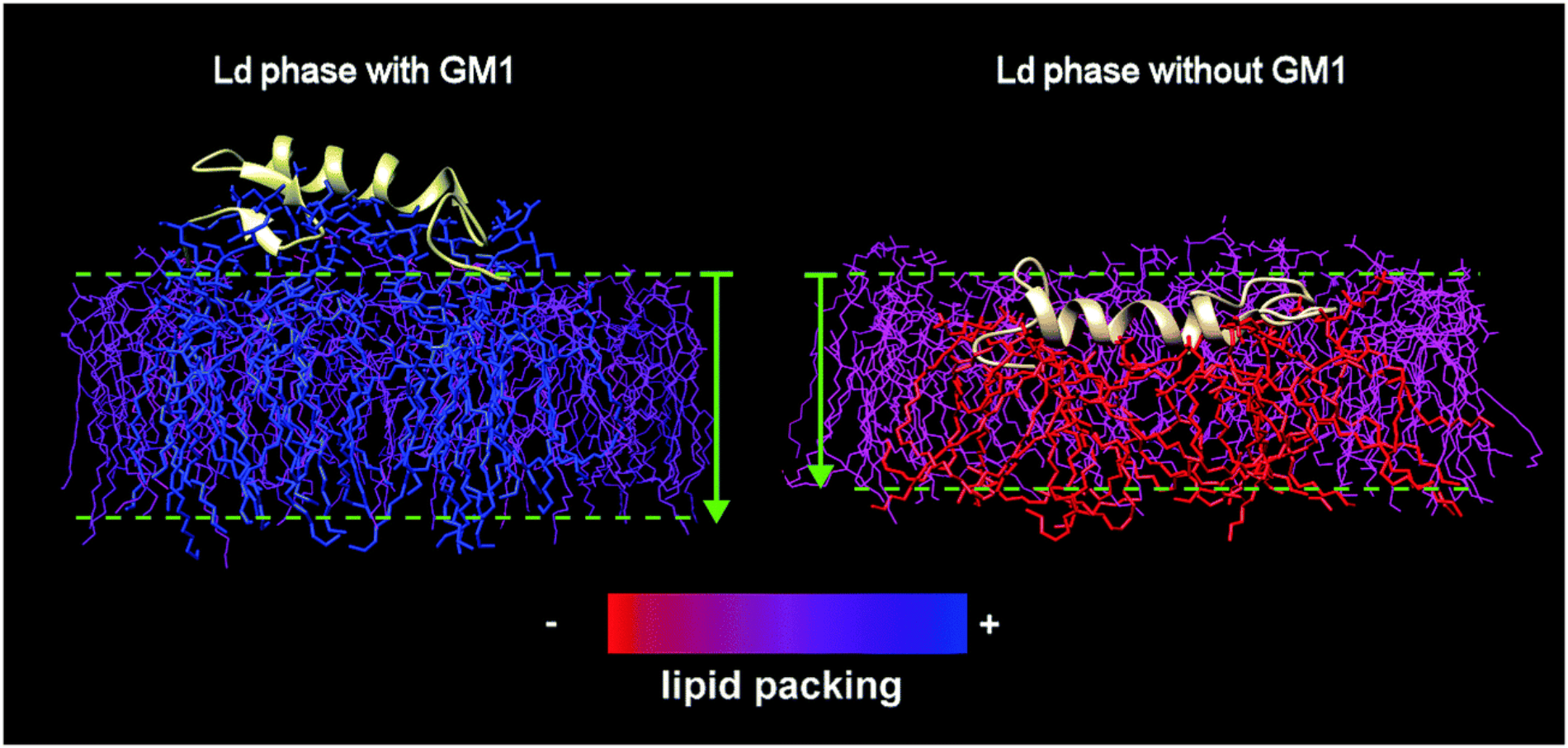
Membranes biologiques et maladie d'Alzheimer
Neurotoxicity and Rheotoxicity: Membrane “Mechanical Toxicity” Hypothesis of Amyloid-β in Alzheimer’s Disease. Vannier F, Thon G, Staneva G , Asnacios S , Puff N, Sorre S, Asnacios A , Angelova MI, 2021. SciMeetings
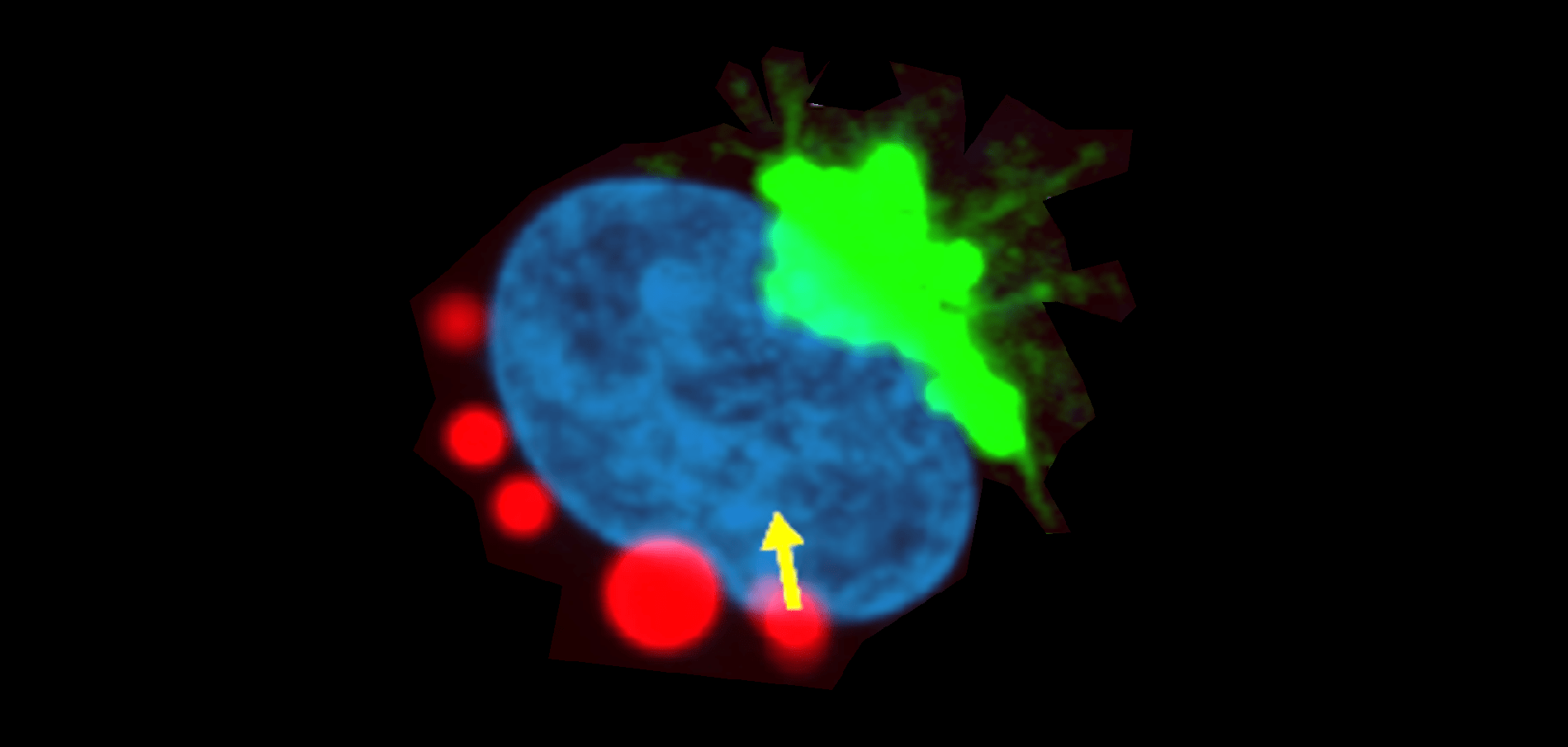
Transport intracellulaire
Nous étudions la mécanotransduction au niveau de l’appareil de Golgi, l’organite au centre du transport intracellulaire. Notre hypothèse est que le Golgi agit comme un senseur de tension qui influence le trafic membranaire intracellulaire. Nous avons montré que l’appareil de Golgi répond à des sollicitations mécaniques internes. Nous nous focalisons maintenant sur l’impact de contraintes externes sur la tension de membrane de l’appareil de Golgi et sur la mécanosensibilité de la voie de sécrétion.
Pour en savoir plus
Quelques articles
Mechanical role of actin dynamics in the rheology of the Golgi apparatus and in Golgi-associated trafficking events
à lire ici
The Golgi apparatus and cell polarity: roles of the cytoskeleton, the Golgi matrix and Golgi membranes
à lire ici
